阶段综合测评(第 7~9 章)
限时:40 分钟 总分:100 分
一、选择题(本大题包括 8 个小题,每小题 6 分,共 48 分。每小题只有一个正确答案)
1.下列生活用品所含的主要材料,属于有机合成材料的是( A )
A.塑料水杯 B.纯棉毛巾
C.羊毛围巾 D.蚕丝被芯
2.下列各组常见的固体物质中,用水不能区分的是( D )
A.NaOH 和 NH4NO3 B.CuSO4和 Na2SO4
C.Na2CO3和 CaCO3 D.NaCl 和 KCl
3.物质 A 可发生下列所示的两个反应,则 A可能是( D )
①A+碱→盐+H2O;
②A+金属氧化物→盐+H2O
A.CaO B.CO2 C.Ca(OH)2 D.HCl
4.推理是化学学习中常用的思维方法,下列推理中正确的是( A )
A.碱性溶液能使紫色石蕊试液变蓝,所以能使紫色石蕊溶液变蓝的溶液一定呈碱性
B.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
C.酸中都含有氢元素,所以含有氢元素的化合物一定是酸
D.酸与碱反应有盐和水生成,因此有盐和水生成的反应一定是酸与碱之间的反应
5.分类是学习和研究化学的常用方法。下列分类中正确的是( B )
A.合成材料:合金、合成橡胶、合成纤维
B.有机物:甲烷、乙醇、葡萄糖(C6H12O6)
C.混合物:煤、石油、冰水共存物
D.复合肥料:尿素、硝酸钾、磷酸氢二铵
6.下列转化不能一步实现的是( C )
A.Ca(OH)2→NaOH B.H2SO4→HCl
C.Fe→Fe(OH)3 D.Cu→Cu(NO3)2
7.下列离子能在 pH=13 的水溶液中大量共存的是( C )
A.SO2-
4 、Cl-、Na
+、H
+
B.K+、SO
2-
4 、Cu2+、NO
-
3
C.Cl-、K
+、SO
2-
4 、Na+
D.Ca2+、Cl
-、CO
2-
3 、Na+
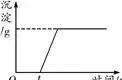
8.某溶液可能含有盐酸、硫酸、硝酸钠、氯化铜中的一种或几种,为了探究其组成,向一定质量的该溶液中
逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。下列相关说法正确的

是( B )
A.加入氢氧化钡溶液至过量,共发生了三个化学反应
B.该溶液一定含有盐酸、氯化铜,可能含有硝酸钠
C.反应过程生成的沉淀一定有氢氧化铜,可能有硫酸钡
D.到达 b 点时所消耗氢氧化钡溶液中溶质的质量是 17.1 g
二、非选择题(本大题包括 4 小题,9~11 题每空 3 分,12 题 10 分,共 52 分)
9.如图是化学反应中的颜色变化,请据图回答:

(1)溶液 X 是__酸__(选填"酸""碱"或"盐"),试剂 A 的名称是__紫色石蕊溶液__。
(2)若 X 是稀硫酸,B为氧化物,则 B 的化学式是__Fe2O3__。
(3)若 X 是稀盐酸,C单质的名称是__铁__。
(4)若 X 是稀硫酸,D是碱,则 X 与 D 反应的化学方程式为__H2SO4+Cu(OH)2===CuSO4+2H2O__。
10.酸奶是日常生活中常见的一种食品,下表是某酸奶外包装上标识的营养成分表。
项目 能量 蛋白质 脂肪 糖类 钠
每 100 g
含量329 kJ 2.6 g 3.1 g 10.0 g 60 mg
请填写下列空格:
(1)酸奶中的__蛋白质__在消化道内会逐渐被分解成可被人体吸收的多种氨基酸。
(2)脂肪在人体内分解、氧化释放出能量的过程,是将__化学__能转化为热能。
(3)蔗糖(C12H22O11)是酸奶中的一种糖类物质,蔗糖的组成中碳、氢元素的质量比为(最简整数比)__72∶11__。
(4)在选择制作酸奶包装盒的材料时,从化学性质的角度分析该材料应具备__无毒__(填写一条即可)的特点。
11.如图是两个实验小组分别进行"加热硫酸铜和氢氧化钠溶液反应后生成物"的实验过程示意图:

【甲组】氢氧化钠与硫酸铜反应的化学方程式为__2NaOH+CuSO4===Na2SO4+Cu(OH)2↓__,加热后产生黑色的
氧化铜。
【乙组】为寻找实验中没有产生氧化铜的原因,他们进行了以下实验探究;
【查阅资料】在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:
6NaOH+4CuSO4===3Na2SO4+Cu4(OH)6SO4↓,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解。
而氢氧化铜能分解:Cu(OH)2=====△
CuO+H2O。
【提出猜想】根据资料分析,同学们针对试管中溶液呈酸性的原因作出以下猜想:
猜想Ⅰ:硫酸铜溶液呈酸性;
猜想Ⅱ:生成的硫酸钠使溶液呈酸性。
【实验与结论】
实验①:用 pH 试纸测定硫酸铜溶液的酸碱度,得出其 pH__<__(选填">""<"或"=")7,硫酸铜溶液呈
酸性,猜想Ⅰ成立。
实验②:向盛有硫酸钠溶液的试管中逐滴滴加石蕊溶液,观察到溶液显紫色,则硫酸钠溶液呈__中__(选填
"酸""中"或"碱")性,猜想Ⅱ不成立。
【交流和反思】
(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立,理由是__甲组实验生成
了 Na2SO4,若它显酸性,在此条件下氢氧化钠与硫酸铜反应会生成蓝白色沉淀__。
(2)在化学反应中,相同的反应物因质量比不同可能会导致生成物不同,请另举一例__炭与氧气__(写出反应
物即可)。
12.某同学在实验室发现一瓶标签残缺的硫酸铜溶液,为了测定此溶液的溶质质量分数,他取出 50 g 该溶
液,向其中逐滴加入溶质质量分数为 20%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量
的关系如图所示。

请你仔细分析此关系图,并进行计算。
(1)当滴入氢氧化钠溶液________g 时,硫酸铜与氢氧化钠恰好完全反应,此时溶液中的溶质为
__________(填化学式)。
(2)计算此硫酸铜溶液中溶质的质量分数(写出解题过程)。
解:(1)由图示可知,当 NaOH 溶液质量为 20 g 时,沉淀不再生成,说明反应恰好完全,此时溶液的溶质为
Na2SO4;
(2)设参与反应的 CuSO4质量为 x。
2NaOH+CuSO4===Na2SO4+Cu(OH)2↓
80 160
20 g×20% x
80
20 g×20%=160
xx=8 g
硫酸铜溶液中溶质的质量分数为:8 g
50 g×100%=16%。
答:此硫酸铜溶液中溶质的质量分数为 16%。
,