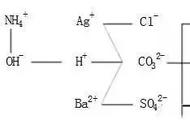
答案为A
2. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是( )
A.NaCl溶液(MgCl2)——加入过量的NaOH溶液,过
滤,滤液中加稀盐酸至中性
B. 氧气(水蒸气)——通过装有足量无水氯化钙的干
燥管
C. CaO固体(CaCO3)——高温充分煅烧
D. 氢气(氯化氢气体)——依次通过足量的NaHCO3溶液和浓硫酸
【解析】氯化镁与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,过滤可除去氢氧化镁沉淀,滤液中加稀盐酸至中性可除去反应剩余的氢氧化钠,得到氯化钠溶液,A方案可行;无水氯化钙具有吸水性,可除去氧气中混有的水蒸气,B方案可行;碳酸钙高温分解生成氧化钙和二氧化碳,采用高温煅烧的方法可除去氧化钙中混有的碳酸钙,C方案可行;氯化氢气体溶于水得到盐酸,碳酸氢钠溶液与盐酸反应生成氯化钠、水和二氧化碳,经过浓硫酸干燥后可得到氢气、二氧化碳的混合气体,除去了杂质氯化氢,但引入了新杂质二氧化碳,D方案不可行。
3. 除去下列各种物质中混有的少量杂质,所用的试剂或操作方法不合理的是( )
选项
物质
杂质
试剂、方法
A
稀硝酸
稀盐酸
适量的硝酸银溶液,过滤
B
木炭粉
铁粉
用磁铁吸引
C
二氧化碳
一氧化碳
点燃
D
氧化铜
铜粉
空气中灼烧
A
√
硝酸银能与稀盐酸反应生成氯化银白色沉淀和稀硝酸,过滤能除去氯化银且没有引入新杂质,符合除杂原则
B
√
铁能被磁铁吸引,可以将杂质除去,符合除杂原则
C
×
大量二氧化碳气体中混有少量的一氧化碳,不能被点燃,不符合除杂原则
D
√
铜在空气中灼烧生成氧化铜,可除去杂质,符合除杂原则
4.为了适应各种不同的需要,常常要把混合物进行提纯:
(1)含有泥沙的粗盐可通过溶解、_____、蒸发等处理,得到初步提纯。其中在蒸发操作中玻璃棒的作用是_____,当蒸发皿中_____________时,停止加热。
(2)除去铜粉中混有的少量铁粉,可采用的物理方法是__________。除去氢氧化钠溶液中的碳酸钠,可以加入适量的_______________________________________________溶液,然后过滤。
【解析】(1)过滤可除去粗盐中的难溶性杂质;蒸发结晶过程中需要使用玻璃棒搅拌,防止局部过热导致液滴飞溅;当蒸发皿中出现较多固体时,停止加热。(2)铁能被磁铁吸引,采用磁铁吸引的方法,可除去铜粉中混有的少量铁粉;碳酸钠与氢氧化钙(或氢氧化钡)溶液反应生成碳酸钙(或碳酸钡)沉淀和氢氧化钠,因此可采用加入适量氢氧化钙(或氢氧化钡)溶液再过滤的方法,除去氢氧化钠溶液中的碳酸钠。

以上就是小编为大家准备的全部内容,谢谢阅览