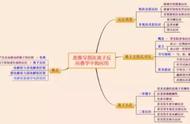
物质氧化性、还原性强弱的比较,实质上是物质得失电子难易程度的比较。即物质越易夺得电子,则其氧化性越强,越难夺得电子则其氧化性越弱;反之,物质越易失去电子,则其还原性越强,越难失去电子,则其还原性越弱。那么话不多说,赶紧拿出小本本记下~

一、利用化合价,比较物质氧化性、还原性强弱
由同种元素形成的不同价态物质的氧化性和还原性的强弱规律是:元素的最高价态只具有氧化性,元素的最低价态只具有还原性,元素的中间价态既有氧化性又有还原性。
例1.对铁元素组成的物质而言:
氧化性:Fe<二价铁盐<三价铁盐
还原性:Fe>二价铁盐>三价铁盐
二、利用元素活泼性的不同,比较物质氧化性、还原性的强弱
1.对金属而言,金属越活泼(金属性越强),其单质的还原性越强,其金属阳离子的氧化性越弱。
例2.对金属活动性顺序表而言:
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
活泼性(金属性)————→减弱
其单质还原性:K>Ca>Na>Mg>Al>…Hg>Ag>Pt>Au
其离子氧化性:K
例3.对同主族的金属元素,从上到下活泼性依次增强。如对ⅡA族金属元素:
Be Mg Ca Sr Ba
活泼性(金属性)————→增强
其单质还原性:Be
其阳离子氧化性:
Be2 >Mg2 >Ca2 >Sr2 >Ba2
例4.对同周期金属而言,从左到右其金属活泼性(金属性)依次减弱。
如对第3周期金属而言:Na Mg Al
活泼性(金属性)————→减弱
其单质还原性:Na>Mg>Al
其阳离子氧化性:Na
2.对非金属而言,其非金属越活泼(非金属性越强),其非金属单质的氧化性越强,其阴离子的还原性越弱。
例5.对一般的非金属活动性顺序而言:F Cl Br I S
活泼性(非金属性)————→减弱
其单质氧化性:F2>Cl2>Br2>I2>S
其阴离子还原性:F-
例6.对同主族的非金属而言,从上到下非金属的活泼性依次减弱。
如对ⅦA族元素而言有:F Cl Br I
活泼性(非金属性)————→减弱
其单质氧化性:F2>Cl2>Br2>I2
其阴离子还原性:F-
例7.对同周期的非金属元素而言,其活泼性从左到右依次增强。
如对第3周期非金属而言:Si P S Cl
活泼性(非金属性)————→增强
其单质氧化性:Si
其阴离子还原性:Si4->P3->S2->Cl-
三、利用氧化还原反应比较物质的氧化性、还原性的强弱

1.对一般的氧化还原反应,氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物。
例8.FeCl3 Cu——→CuCl2 FeCl2
氧化剂 还原剂 氧化产物 还原产物
氧化性比较:Fe3 >Cu2 还原性比较:Cu>Fe2
例9.FeCl2 Cl2——→FeCl3
还原剂 氧化剂 氧化产物,还原产物
氧化性比较:Cl2>Fe3 还原性比较:Fe2 >Cl-
综合例8和例9有:
其氧化性比较:Cl2>Fe3 >Cu2 其还原性比较:Cu>Fe2 >Cl-
2.对原电池反应而言,均有:还原性比较:负极材料>正极材料;
氧化性比较:负极失去电子形成的阳离子<正极上得到电子的阳离子(或氧化剂)。
例10.用导线连接的铜锌二极,插入到CuSO4溶液中,可形成原电池。
负极(Zn):Zn——2e=Zn2 (氧化) 正极(Cu):Cu2 2e=Cu(还原)
氧化性比较:Cu2 >Zn2 还原性比较:Zn>Cu
例11.Fe-C合金在中性溶液中存在时,Fe易发生吸氧腐蚀,本质上属原电池反应。
负极(Fe):Fe-2e=Fe2 (氧化) 正极(C):2H2O O2 4e=4OH-(还原)
氧化性比较:Fe2 还原性比较:Fe>C
例12.Fe-Cu合金在酸性较强的介质中铁先被腐蚀,此为析氢腐蚀,本质上也属原电池反应。
负极(Fe):Fe-2e=Fe2 (氧化) 正极(Cu):2H 2e=H2↑(还原)
氧化性比较:H >Fe2 还原性比较:Fe>Cu
3.对电解反应而言,同一电解质溶液中,电解时,在阳极越易放电(失电子)的阴离子,其还原性越强;阴极上越易放电(得到电子)的阳离子,其氧化性越强。
如在一般浓度的电解质混合溶液中,在阳极的各离子放电顺序一般有:S2->I->Br->Cl->OH->F-
则其还原性比较:S2->I->Br->Cl->OH->F-
在阴极的各离子放电顺序:
Au >Pt2 >Ag >Hg2 >Cu2 >H >…
则其氧化性比较:
Au >Pt2 >Ag >Hg2 >Cu2 >H >…
四、用同一起点反应进行的难易程度来比较物质氧化性、还原性的强弱
1.与同一还原剂的反应越易进行,其氧化剂的氧化性越强(说明越易夺得电子)。
从反应的条件看,与同一还原剂铜反应时,浓硝酸比浓硫酸易于发生。
氧化剂氧化性比较:浓硝酸>浓硫酸
从反应条件看,与同一还原剂Cu反应时,浓HNO3比稀HNO3易于发生。
氧化剂氧化性比较:浓HNO3>稀HNO3
2.与同一氧化剂的反应越易进行,其还原剂的还原性越强(说明越易失去电子)。
例15.从与同一氧化剂浓HNO3反应的条件可以看出,C与浓HNO3的反应比Cu难以发生。
还原剂还原性比较:Cu>C
最后,为了方便同学们记忆,小编教给大家一条记忆口诀:升失氧(化合价升高,失去电子,被氧化),降得还(化合价降低,得到电子,被还原),得氧剂(得到电子是氧化剂),失还剂(失去电子是还原剂),希望同学们在看了以上整理后对氧化反应有更深入的认识,能够灵活运用到日常的解题中。