摘自微信公众号“血液透析那些事儿”,原作:协和麒麟医学。
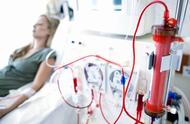
对于肾衰竭和严重急性肾损伤(AKI)患者,血液透析是挽救生命的急先锋,也是维持生命的守护神。

虽然治疗过程复杂,需要建立和维护血管通路、进行体外血液循环、使用相应的药物,但幸运的是,随着技术方案和指导规程的不断优化,血透治疗整体相当安全,严重的并发症并不常见。
然而,仍有些并发症是由于人为疏忽而发生的,也因此是可以预防和避免的,怎样及早识别和预防,而不是事后反思和遗憾?
本期,AJKD杂志发表了一篇文章,将透析器反应、透析失衡综合征、尿毒症/透析相关的心包炎、空气栓塞、静脉针脱落、血管通路出血、溶血、透析水污染和心律失常发作共9种血液透析紧急情况,在互动病例场景中,完成实战解答指导。

如果在临床中遇到这些突发情况,你知道对应的解决方案吗?跟随协和麒麟医学一起,一探究竟吧~
一表总结

一、透析器反应和其他过敏性反应
病例1:一位68岁的女性,患有高血压、糖尿病和CKD5期,由于对利尿剂不耐受而开始使用血液透析。第一次治疗10分钟后,她报告全身瘙痒、呼吸困难和胸痛,医生注意到她有明显的喘息声。她的血压降为86/50 mmHg(透析开始前为145/90 mmHg),怀疑透析器反应。
问题1:对该患者的管理,下一步应该采取什么措施?
a) 继续透析并静脉注射抗生素
b) 继续透析并通过雾化器给予阿布特罗
c) 继续透析,静脉注射皮质类固醇和抗组胺药
d) 停止透析,将体外循环中的血液回输给患者
e) 停止透析,不将体外循环中的血液回输给病人
您知道正确答案吗?
正确答案是(e)。根据需要使用液体、肾上腺素、皮质类固醇和抗组胺药。
透析器反应是对膜本身或膜消毒产品的超敏反应。有报告称,常见过敏反应发生在以下材料的透析器上:铜铵薄膜,一种过去比较常用的纤维素膜;丙烯腈,一种合成膜,在服用血管紧张素转换酶抑制剂(ACEI)的病人中引起急性反应;以及聚砜或聚醚砜,这是最常用的合成膜。过去常用于消毒透析膜的环氧乙烷和用于再处理透析器的甲醛,在使用后没有充分冲洗透析器,导致病人接触到这些物质。
透析器反应以前被称为"首次使用综合症",因为它们通常出现在第一次使用透析器时,尽管透析器反应曾经相当普遍,但由于生物相容性膜的使用增加和环氧乙烷灭菌的使用减少,现在已经很少见了。
透析器反应分为A型、B型两类。A型反应发生在治疗的早期,通常在头20至30分钟内。它们通常发生在第一次治疗期间,但也可能在多次治疗后发生。体征和症状可能包括瘙痒、荨麻疹、喉头水肿、支气管痉挛、呼吸困难、胸痛、呕吐、缺氧、低血压和心脏骤停。对严重反应的处理包括停止透析,而不将血液从体外循环中回流到患者体内。
B型反应发生在治疗的后期,而且不太严重。症状可能包括胸痛和背痛、恶心和呕吐。如果症状轻微,可以继续透析,不过应考虑换用不同的透析器。
大多数A型反应被认为是由环氧乙烷、甲醛和使用丙烯腈透析器与ACEI引起的,其中环氧乙烷占大多数。
铜铵薄膜和聚砜/聚醚砜可以激活补体,这被认为是B型反应的主要原因。然而,在接触聚砜透析器的病人中,也有IgE水平升高的严重反应的报道。测量总IgE和胰蛋白酶(过敏性休克时肥大细胞释放的一种蛋白酶)可能有助于确定是由过敏性休克还是其他原因造成的。
超敏反应也可见于透析期间使用的药物,包括肝素、静脉注射铁剂和促红细胞生成剂。处理方法包括避免使用引起反应的药物、使用替代物。
二、透析失衡综合征
病例2:一位75岁的男性,患有高血压、糖尿病、CKD和缺血性中风病史,因恶心、食欲下降和高钾血症而开始接受透析。他透析前的实验室值为:血清肌酐(Scr),10.1 mg/dL;血清尿素氮,170 mg/dL;钠,128 mEq/L;钾,7.2 mEq/L;碳酸氢盐,12 mEq/L;葡萄糖,101 mg/dL。透析处方治疗时间为2小时,血流量为400毫升/分钟,透析液流量为800毫升/分钟,透析液为标准钠,目标超滤为2升。使用的是低效率的透析器。他的透析过程并不顺利,直到治疗结束时,他报告出现了新的头痛症状。他的血压145/96mmHg,在治疗过程中稳定,随后他出现了癫痫发作,透析立即停止。
问题2:如何改变处方以减少透析失衡综合征的风险?
a) 降低超滤目标
b) 降低透析液的钠浓度
c) 减少血流量
d) 增加治疗时间
您知道正确答案吗?
正确答案是(c)。
透析失衡综合征(DDS)的特点是在血液透析过程中或结束后不久出现的神经系统体征和症状。临床表现可包括头痛、恶心/呕吐、精神错乱、激动、癫痫发作、昏迷,甚至死亡。在CT和MRI上可以看到脑水肿。
DDS通常见于接受首次透析治疗的血清尿素氮(SUN)显著较高的患者。其他风险因素包括血清尿素氮快速降低、年龄极大或极小、代谢性酸中毒、低钠/高钠血症、肝脏疾病和既往已发生的神经系统疾病。近几十年来,由于临床实践的改变,如以较低的血流速度和较低的SUN水平开始透析,DDS的发病率已经下降,目前发生率已较低,尽管可能在症状较轻的患者中未被充分认识。
DDS中出现的脑水肿是由水进入脑细胞引起的,最普遍的理论是"反向尿素效应"。另外,在尿毒症大鼠的大脑中观察到水蛋白AQP4和AQP9的表达增加,尿素转运体UT-B1的表达减少,这表明尿毒症可能会增加大量水流动的风险。自发性渗透溶质和脑内酸中毒也被认为是可能的机制。
治疗取决于症状的严重程度。如果在透析期间出现DDS的相关症状,应停止治疗。轻度的症状可以进行支持性管理。对于严重的症状,可以采用降低颅内压的措施。
而采取短时间内减少SUN不超过40%来预防DDS是至关重要的。建议在2小时内使用200毫升/分钟的低血流量启动HD(甚至更少,取决于病人的体型)。
当维持性透析患者的SUN明显升高时,也建议使用较低的血流量。对于SUN非常高的患者,应考虑使用连续肾脏替代疗法(CKRT)缓慢降低SUN。另一种方法是提高血液或透析液的渗透压,以减少透析时渗透压的变化。据报道,使用较高钠的透析液可以防止DDS的症状。其他已经使用的药剂包括甘露醇、葡萄糖、甘油和尿素。
三、尿毒症心包炎
CKD患者的心包炎被分为尿毒症心包炎(定义为在开始透析前或8周内发生)或透析相关的心包炎(定义为在透析8周后发生)。
尿毒症心包炎比过去要少得多,但尿毒症和透析相关的心包炎仍然是肾衰竭患者心包疾病的最常见原因。在透析人群中引起心包炎的其他原因包括感染、自身免疫性疾病、恶性肿瘤、外伤和心肌梗塞。