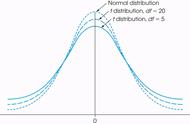
蛋白质进入线粒体示意图[6]
1988年,哈特尔的导师诺佩特给霍里奇打了一个越洋电话。霍里奇几乎放下电话就去买了飞往慕尼黑的机票。[5]
面对霍里奇带来的结果,诺佩特和学生们尽管感到很兴奋,却依旧保持怀疑 —— 如果要证明存在一种辅助OTC折叠的蛋白质,必须要证明 OTC 完全进入了线粒体,因为OTC可能在穿过线粒体膜的过程中“卡住”,而这种情况下呈打开状态的OTC可能会被从中切断而失去活性。—— 这时,哈特尔主动请缨,自己来做这个实验。
仅仅几周,哈特尔就做出实验结果—— OTC的确完全进入了线粒体。这意味着,线粒体内确实存在一种折叠酶(foldase)。哈特尔、霍里奇以及诺佩特等人于1989年在 《自然》上发表了两篇标志性论文 [7-8]:安芬森法则统治蛋白质折叠的时代结束了。
哈特尔在32岁用了几个星期做出了让他在日后蜚声科学界的工作。

文献 [7] 证明一种名为hsp60的线粒体内的热休克蛋白在进入线粒体的蛋白的组装过程中起关键作用。因为 hsp60 符合约翰·埃利斯(John Ellis)在1987年对 “分子伴侣”(molecular chaperone)的定义,所以被归纳为一种分子伴侣蛋白。[9] 这篇论文的首作者郑明媛(CHENG Ming Y.,右上角)是霍里奇的最早的研究生之一, 现已从台湾省国立阳明大学生命科学系暨基因体科学研究所退休。霍里奇形容她为 “无所畏惧的实验学家”。[10-11]

文献 [8] 则进一步证明线粒体内的蛋白质折叠必须要hsp60,并且消耗ATP水解的能量。
分子伴侣:热休克蛋白哈特尔和霍里奇一同荣获过许多奖项,包括2011年的拉斯克基础医学研究奖。荷兰遗传学细胞生物学家、洛克菲勒大学教授蒂蒂亚·德朗厄(Titia de Lange)是二人获得拉斯克奖的现场介绍人。
德朗厄在介绍二人获奖工作时做了一段很精妙的比喻,来说明热休克蛋白hsp60的功能:
“Hsp60体系像一座监狱能够将蛋白质囚禁在单人牢房—— 这就像是美国的监禁制度(American penal system),只是去掉了无人道的(inhumane)部分,并且更加高效。Hsp60形如圆桶,抓住去折叠蛋白分子的黏性部分,将之拽入桶内,并关闭桶盖。此时陷入hsp60的蛋白分子尝试各种姿态构象进行折叠,而不必碰撞其它蛋白质分子。Hsp60的桶壁高度带电。蛋白质分子被关押在桶内约10秒,可以想象,它在此过程中挣扎、扭动,碰撞墙壁,直至桶门打开。越狱犯可能完成了正确折叠,成为了细胞内茫茫蛋白中的一位好好公民,也可能还没有完成折叠。那么这样的累犯会迅速被捕获、押解入另一个囚笼。这个先擒后纵的过程可能往复十次,才最终令一条多肽链正确折叠,进而获得保释,允许出狱,如同一个模范公民,去履行自身的职责,再也不与其它蛋白质分子有非分接触。”
“哈特尔和霍里奇的工作大大加深了我们对细胞生命功能的理解,在医学、药学方面有广泛应用。几乎所有蛋白质在其熟化(maturation)过程中都需要分子伴侣的某种形式的参与,而几乎所有生命体都使用 “单独囚禁” 的方式驱策它们的一部分蛋白正确折叠。分子伴侣-辅助的蛋白质折叠给我们提供许多洞见,以理解因蛋白变异而导致的疾病,如阿尔茨海默症、帕金森症、卢·贾里格症(又称肌萎缩性脊髓侧索硬化症、渐冻症)等。” [6]

Hsp60-Hsp10 分子伴侣复合体功能示意图[12]
哈特尔的学术家谱笔者叙述科学家事迹有一个习惯:总免不了考察他的学术家谱。哈特尔是德国培养的科学家,在当前美国的生命科学整体领先欧洲及东亚的大背景下,追索一下他的师承脉络,可能会给我们带来一些有益的启发。
哈特尔的学术生涯里先后有三位导师:博士导师、化学家、海德堡大学医学院教授 Hans Schimassek,博后导师、细胞生物学家、慕尼黑大学教授瓦尔特·诺佩特,博后导师、生物化学家、达特茅斯学院教授威廉姆·维克纳(William T. Wickner)[12]。
哈特尔曾自述在诺佩特教授处的经历是其人生重大转折,那么我们重点攀着诺佩特的师承谱系树上行看一看。