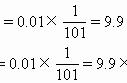类型2 水的离子积常数(Kw)
1.概念:水或稀溶液中c(H+)与c(OH-)的乘积。
2.表达式:Kw=c(H+)·c(OH-)。
3.影响因素:温度(升温,Kw增大)
4.常见题型
(1)计算[计算Kw、c(H+)、c(OH-)、pH]。
(2)通过Kw的大小比较,判断相应温度的高低。
[对点训练]
4.T ℃下的溶液中,c(H+)=10-x mol·L-1,c(OH-)=10-y mol·L-1,x与y的关系如图所示。下列说法不正确的是( )

A.T ℃时,水的离子积Kw为1×10-13
B.T>25
C.T ℃时,pH=7的溶液显碱性
D.T ℃时,pH=12的苛性钠溶液与pH=1的稀硫酸等体积混合,溶液的pH=7
D [从图看出当c(H+)=10-13 mol·L-1时,c(OH-)=100 mol·L-1=1 mol·L-1,故T ℃时,Kw=1×10-13,A正确;T ℃时,Kw大于1×10-14,则T ℃一定高于常温,B正确;T ℃时,pH=6.5的溶液呈中性,显然pH=7的溶液显碱性,C正确;pH=12的苛性钠溶液与pH=1的稀硫酸等体积混合,二者恰好完全中和,但注意该温度下,pH=7的溶液不是中性溶液,D错误。]
5.水的电离平衡曲线如图所示。下列说法正确的是( )

A.a点对应温度条件下,将pH=x的氨水稀释10倍后,其pH=y,则x=y+1
B.纯水仅升高温度,可从d点变到b点
C.c点对应温度条件下醋酸的电离常数比a点对应温度条件下醋酸的电离常数大
D.b点对应温度条件下,0.5 mol·L-1的H2SO4溶液与1 mol·L-1的KOH溶液等体积混合,充分反应后,所得溶液的c(H+)=10-7 mol·L-1
C [A项,NH3·H2O是弱电解质,加水稀释促进NH3·H2O的电离,将pH=x的氨水稀释10倍后,溶液中的OH-浓度大于原来的eq \f(1,10),则x<y+1,错误;B项,d点和b点的c(OH-)相等,若纯水仅升高温度,c(OH-)与c(H+)都增大,错误;C项,水的电离是吸热反应,温度升高,水的离子积增大,根据图中数据得出各点对应的水的离子积Kw的数值大小关系为b>c>a=d,温度关系为b>c>a=d,而醋酸的电离也是吸热反应,温度越高,电离常数越大,正确;D项,b点的Kw=1.0×10-12,0.5 mol·L-1的H2SO4溶液与1 mol·L-1的KOH溶液等体积混合,充分反应后所得溶液呈中性,此时c(H+)=1.0×10-6 mol·L-1,错误。]
类型3 溶度积常数(Ksp)

[对点训练]
6.(2016·威海质检)已知常温下:Ksp[Mg(OH)2]=1.8×10-11;Ksp(AgCl)=1.8×10-10;Ksp(Ag2S)=6.3×10-50;Ksp(CH3COOAg)=2.3×10-3。下列叙述不正确的是( )
A.常温下,浓度均为0.02 mol·L-1的AgNO3溶液和CH3COONa溶液混合一定产生CH3COOAg沉淀
B.常温下,将0.001 mol·L-1的AgNO3溶液加入到浓度均为0.001 mol·L-1的KCl和K2S的混合溶液中,先产生Ag2S沉淀
C.常温下,调节溶液的pH>9,能使Mg2+浓度为0.12 mol·L-1的溶液中产生Mg(OH)2沉淀
D.常温下,向饱和AgCl溶液中加入NaCl溶液,Ksp(AgCl)不变
A [选项A中没有说明两者按什么样的体积比混合,若按体积比1∶1混合,则c(Ag+)·c(CH3COO-)=0.01×0.01=10-4<Ksp(CH3COOAg),故没有沉淀生成,A错误;虽然Ag2S和AgCl中阴、阳离子个数比不同,但因Ksp(Ag2S)=6.3×10-50≪Ksp(AgCl)=1.8×10-10,故先产生Ag2S沉淀,B正确;调节溶液的pH>9,则c(OH-)>1×10-5 mol·L-1,c(Mg2+)·c2(OH-)>1.2×10-11,即c(Mg2+)·c2(OH-)>Ksp[Mg(OH)2],故产生Mg(OH)2沉淀,C正确;Ksp只与温度有关,D正确。]
已知:Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。向浓度均为0.01 mol·L-1的Cu2+和Mg2+的混合溶液中逐滴加入NaOH溶液至过量,下列说法正确的是( )