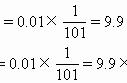与Na2CO3溶液充分反应后,生成Na2MoO4和另外一种物质,该物质的电子式为 。粗产品经过充分碱浸后所得的碱浸液中部分离子的浓度:c(
)=0.40 mol·L−1,
c(
)=0.05mol·L−1。结晶前应先除去
,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当BaMoO4开始沉淀时,
的去除率为 。
[已知:Ksp(BaSO4)=1.1×10−10,Ksp(BaMoO4)=4.0×10−8]
(3)该流程中操作2为过滤,如果在实验室模拟该操作时,发现滤液中有少量浑浊,从实验操作的角度分析,可能的原因是 。
(4)重结晶得到的母液可以在下次重结晶时重复使用,但达到一定次数后必须净化处理,原因
。
(5) 工业上由MoO3制备Mo粉也常用铝热反应,写出该反应的方程式 。
(6)操作3在碱性条件下,将钼精矿加入到足量的NaClO溶液中,也可以制备钼酸钠。该反应的离子方程式为 。
12、“钢是虎,钒是翼,钢含钒犹如虎添翼”,金属钒被誉为“合金的维生素”。从废钒(主
要成分为V2O5、Fe2O3、SiO2等)中回收V2O5的一种工艺流程如下图所示:

已知:步骤②、③中的变化过程可简化为:Rn (水层) nHA(有机层)
RAn(有机层) nH (水层)(式中Rn 表示VO2 或Fe3 ,HA表示有机萃取剂)。
回答下列问题:(1)步骤①酸浸过程中发生氧化还原反应的化学方程式为______________。
(2)萃取时应加入适量碱的作用是___________________。
(3)步骤④中反应的离子方程式为___________________。
(4)步骤⑤25°C时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
通过表中数据分析,在实际生产中,⑤中加入氨水,调节溶液的最佳pH范围为______;
若加入氨水调节溶液pH=2,钒沉淀率达到93%且不产生Fe(OH)3沉淀,则此时溶液中c(Fe3 )<_____mol/L(按25℃计算,25℃时Ksp[Fe(OH)3]=2.6×10-39)。
(5)V2O5是两性氧化物,在强酸性溶液中以VO2 形式存在,VO2 具有强氧化性,能将I-氧化为I2,本身被还原为VO ,则V2O5与氢碘酸反应的离子方程式为_________________。
(6)为提高钒的回收率,步骤②和③需多次进行,假设酸浸所得“强酸性浸出液”中c(VO2 )=amol/L,步骤②和③每进行一次,VO2 萃取率为80%,4次操作后,“强酸性浸出液中”c(VO2 )=_______mol/L(萃取率=