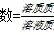同样重要的几个公式还有,物质的量=质量/摩尔质量=粒子数/阿伏伽德罗常数=气体体积/气体摩尔体积=溶液物质的量浓度×溶液体积。
稀释定律:=, =
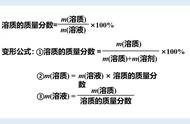
另外我们还需要掌握常用公式的变形,=/ =/(( ))
=/( )×%相关推导过程在前面的课程中已经讲过,记不清楚的话可以回过头去再复习一下。

(2)注意
相关物理量在进行相互换算时,都要经过“立交桥”的中枢,即物质的量。
应用气体摩尔体积等于22.4 L/mol时,必须是标准状况下。
另外还要注意一些特殊情况:
比如特殊物质存在状态,例如SO3标况下为固体,CCl4、C2H5OH、H2O等在标况下为液体。

又比如特殊的物质组成,例如盐酸是HCl的水溶液,等物质的量的CO与NO含有相同的原子数,等质量的NO2和N2O4含有相同的原子数等。
我们在做题时要特别注意这些容易被忽略的陷阱。

(3)典型例题,判断对错,请各位同学先暂停视频,自己先尝试判断。
我们一起来看,第一题,常温常压下,14 g N2和CO组成的混合气体含有原子数为NA。氮气和一氧化碳的摩尔质量都是28 g/mol,所以14 g N2和CO组成的混合气体是0.5 mol,并且和温度压强无关,更巧的是氮气和一氧化碳都是双原子分子,所以混合气体中不论N2和CO以什么比例混合,其中的原子数都是NA个。所以这道题是正确的。
第二题,常温常压下,8 g O2含有2NA个电子 。在做这道题的时候要注意审题,题目中问的是O2中有几个电子,不能惯性思维的当成问几个原子,更不能想当然的认为是成键电子或者是电子对。8 g氧气是0.25 mol,而O2共有16个电子,因此共有电子0.25×16=4 mol。也就是4NA个电子。因此这道题错误。
第三题,标准状况下,22.4 L盐酸含有NA个HCl分子。这道题考查的就是我们刚刚提到的要注意特殊的物质组成,盐酸是HCl的水溶液,因此题目中的说法肯定是错误的。
来看最后一题,已知C2H4和C3H6的混合物质量为a g,则该混合物所含原子总数为/。我们来分析题目,C2H4和C3H6的相对分子质量并不相同,但是都有由(CH2)这个基本单元组成,那么我们可以将(CH2)看作一个整体来进行分析。a g混合物中有(CH2)a/14 mol,而每个(CH2)单元有3个原子,因此a g混合物中应该有3a/14 mol 原子,即3aNA/14个原子。所以题目中的说法不正确。