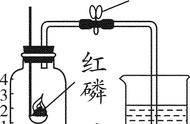
过滤适用于液体和固体混合物的分离。
操作要点:" 一贴、二低、三靠 " 。
一贴:滤纸紧贴漏斗内壁。
二低:①滤纸边缘要低于漏斗的边缘;
②待过滤的液体要低于滤纸的边缘。
三靠:①倾倒液体的烧杯紧靠引流的玻璃棒;
②玻璃棒下端要紧靠三层滤纸处;
③漏斗的下端要紧靠烧杯内壁。
备注:
滤纸紧贴漏斗内壁。-----为了加快过滤速度。
滤纸边缘要低于漏斗的边缘------防止滤纸被水润湿后破损
液体面要低于滤纸的边缘。------防止液体从滤纸与漏斗间流下,使过滤不充分
倾倒液体的烧杯紧靠引流的玻璃棒------防止液体溅出
玻璃棒下端要紧靠三层滤纸处-------防止玻璃棒戳穿滤纸
漏斗的下端要紧靠烧杯内壁。-------防止液体溅出
过滤后仍然浑浊的原因:
A、滤纸破损
B、液面高出滤纸边缘
C、承接滤液的烧杯水不干净
6、蒸馏操作技巧
①在加热时,烧瓶中应放入几粒沸石(碎瓷片),防止暴沸;
②刚开始蒸馏出的液体不能要,因为有些杂质混在水中,蒸馏开始会先蒸馏出来;
③注意温度要指在100℃。
④温度计的水银泡要在蒸馏瓶的支管处;
⑤冷凝管内的水流从下往上。
课题3:水的组成
水的物理性质
水是无色、无味的液体。在4℃时,水的密度最大为1g/cm3。在101kPa下,水的凝固点为0℃(结冰),沸点是100℃。冰的密度比水的密度小。水的导电能力较弱。
1、

水的电解实验
(1)实验装置:水的电解装置如图所示。
(2)实验现象:通电后,电极上有气泡产生,通电一段时间后,两个玻璃管内汇集了一些气体,与正极相连的玻璃管内的气体体积小,与负极相连的玻璃管内的气体体积大,体积比约为1:2。
检验气体:体积小的气体能使带火星的木条复燃,证明是氧气;体积大的气体燃烧能产生淡蓝色火焰,证明是氢气。
实验结论:水是由氢元素和氧元素组成的。水在通电条件下,发生分解反应,产生氢气和氧气。
化学方程式为:

2、氢气的制法、性质和用途
氢气的实验室制法
(1)反应原理:锌和稀硫酸反应产生氢气。
Zn+H2SO4=ZnSO4+H2↑
(2)实验室制取氢气的装置
实验室制取氢气的反应是块状固体和液体之间的反应,不需要加热。有关装置如图所示。

(3)操作步骤:
①按要求装配好仪器;②检查装置气密性;
③装药品;④验纯;⑤收集气体。
(4)收集方法:①向下排气法;②排水法。
(5)验纯:用拇指堵住集满氢气的试管口,靠近火焰,移开拇指点火,听到尖锐的爆鸣声,表明氢气不纯,声音较小,表明氢气较纯。
(6)放置:倒放在桌面上,因为氢气的密度比空气小。
(五)物质的分类
化合物:由不同种元素组成的纯净物叫化合物。
单质:由同种元素组成的纯净物叫单质。
氧化物:由两种元素组成的化合物中,其中一种元素是氧元素的叫做氧化物
课题4:化学式与化合价
1、化学式:用元素符号和数字的组合表示物质的组成的式子叫做化学式。
①纯净物的化学式只有一个。(纯净物固定的组成,可以用化学式表示,混合物没有化学式)
②书写物质化学式时应以事实为基础,不能任意书写。(每个化学式都有各自的含义
③单质在书写化学式时,注意:
稀有气体:用元素符号表示 如:氦He 氖Ne
金属和固体非金属:习惯上用元素符号表示 如:铁 Fe 碳 C
非金属气体单质:在元素符号右下角写上表示分子中所含原子数的数字如O2、N2
2、化学式表示的含义:
3、化学符号中数字的意义。
①元素符号前的数字表示原子个数,如3H,表示3个氢原子。
②化学式前的系数表示该物质的分子个数。如3H2SO4,表示3个硫酸分子。
③写在元素符号右上角的数字,表示该元素的离子所带的电荷数,数字之后的" "、"-"是表示离子所带的电性。如Mg2 表示一个镁离子带两个单位的正电荷(数字在前,正、负号在后)。
④写在化学式中元素符号右下角的数字,表示一个分子中所含的原子个数。如H2O中"2"表示1个水分子中含有2个氢原子。]
4、化合物在书写化学式时,注意:
(1)当某组成元素的原子个数比为1时,1可省略。如 CO、MgO等。
(2)氧化物化学式书写,一般要"某前氧后"。如CO2、P2O5、Fe3O4等。
(3)有金属元素和非金属元素组成的化合物,书写时,一般把金属元素符号写在左方,非金属元素的符号写在右方。如 NaCl 即:"金前非后"
5、化合价:一种元素一定数目的原子跟其他元素一定数目的原子化合的性质,叫做这种元素的化合价。即原子间重新组合时,有固定的原子个数比。
(1)化合价是元素在形成化合物时,才表现出来。故单质的化合价为零价。
(2)化合价的一般规律:
(a)金属只显正价,非金属有正价和有负价。
(b)氢为 1价,氧为-2价。
(c)许多元素有变价。
(d)在化合物中元素正负化合价的代数和为零。
(e)在单质中元素的化合价为零价。
(f)元素的最高正价=最外层电子数(氧、氟无正价); 最低负价=最外层电子数减8
(3).元素化合价的表示方法:化合价用 1、 2、 3、-1、-2…表示,标在元素符号的正上方,如:Na、 Cl、 Mg、 O。要注意化合价的表示方法与离子符号的区别,离子所带电荷符号用 、2 、-、2-…表示,标在元素符号的右上角,如:Na 、Cl-、Mg2 、O2-。
6、元素化合价规律记忆表:
7、原子、离子及化合价三者之间的*
8、化合价与离子符号的比较:
9、物质化学式的书写:一、单质
1、【"A"型】
2、【"A2"型】
二、化合物
1、氧化物:由两种元素组成的化合物中,其中一种元素是氧元素的叫做氧化物
①【"读法特殊"型】
⑴水: H2O ;⑵过氧化氢(双氧水):H2O2
②【"几氧化几某"型】
③【"氧化某"型】
2、酸:( 酸==H 酸根离子 )
3、碱: 氢氧化某 (碱==金属离子 OH- )
氢氧化钙的俗称有: 熟石灰 、 消石灰 。
4、盐:某化某、 某酸某 (盐==金属离子 酸根离子 )
三、根据化学式的计算
(1)求物质的相对分子质量
将化学式中所有的原子的相对原子质量总和,就是相对分子质量(符号 Mr )
如:Ca(OH)2 : Mr[Ca(OH)2]==40 2×(16 1)=74
(2)求化合物中各原子个数之比
在化学式中,元素符号右下角的数字就是表示该元素原子的个数,因此这些数字的比值就是化合物中的原子个数如:Fe2O3中,铁原子与氧原子个数比就是2:3,碳酸钙CaCO3中钙、碳、氧原子个数比为1:1:3
但注意某些物质的化学式中,同种元素并不写在一起的,这时要注意原子个数
如:NH4NO3中,氮、氢、氧原子个数比应该为2:4:3
Cu2(OH)2CO3中,铜、碳、氢、氧原子个数比为2:1:2:5
(3)求化合物中各元素质量之比(易错点-把个数比看成质量比)
在化合物中,各元素质量之比就是各元素的原子个数与它的相对原子质量积之间的比值
如:氯酸钾(KClO3)中,
m(K)︰m(Cl)︰m(O)=39︰35.5︰16×3=78︰71︰96
硝酸铵(NH4NO3)中,
m(N)︰m(H)︰m(O)=14×2︰1×4︰16×3=7︰1︰12
(4)计算化合物中某一元素的质量分数
元素的质量分数(ω)=×100% (熟记
如:计算MgSO4中氧元素的质量分数