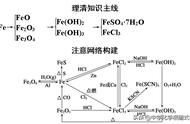
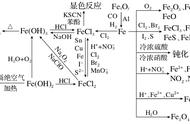
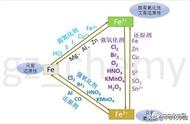
(5)Fe3 ---> Fe2
铁盐溶液与某些还原剂(如Fe、Cu、I-、S2-等)反应。如:
2Fe3 S2-= 2Fe2 S↓
2Fe3 Cu= 2Fe2 Cu2
2Fe3 Fe= 3Fe2
2Fe3 2I-= 2Fe2 I2
(6)Fe2 ---> Fe
亚铁化合物与比较活泼的金属(如Al、Zn)、CO、H2、C等反应。如:

2、“铁三角”的应用
1)、判断离子共存
- ①Fe2 与 NO3-(H )、ClO-、MnO4-(H )不共存(因氧化还原反应)。
- ②Fe3 与 S2-、I-、SO32-、HSO3-不共存(因氧化还原反应)。
- ③Fe2 、Fe3 与HCO3-、CO32-、AlO3-等不共存(因发生相互促进的水解反应)。
2)、除杂(括号中为杂质)
- ①Fe2 (Fe3 ):加过量铁粉,过滤。
- ②FeCl3(FeCl2):加氯水或H2O2溶液。
- ③FeCl2(CuCl2):加过量铁粉,过滤。
- ④Fe(Al)、Fe2O3(Al2O3、SiO2):加过量强碱溶液,过滤。
- ⑤Cu2 (Fe3 ):加CuO或Cu(OH)2或Cu2(OH)2CO3调节pH至3.7左右。
3)、盐溶液的保存

4)、物质制备

特别提示:Fe2 具有较强的还原性;Fe3 水解能力强,pH>3.7时,Fe3 几乎完全水解生成Fe(OH)3沉淀。欲除去某溶液中含有的Fe2 杂质,一般先向溶液中加入氧化剂(如H2O2),将Fe2 氧化为Fe3 ,然后加碱或盐调节pH,使Fe3 转化为Fe(OH)3沉淀而除去。
往期链接:点击直达
5、
6、
7、
8、
9、
如果您喜欢,可以收藏、点赞加关注,您的支持,是我继续推出文档的动力!
网页版,排版不太好,想要文字word文档的,请私信我!