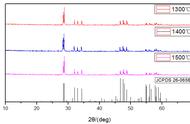
银元素是一种化学元素,其化学符号为Ag,原子序数为47。它是一种贵金属,因为它的产量较少,同时它在电气、光学和医学等领域中具有广泛的应用。
纯白银颜色白,金属光泽,质软,掺有杂质后变硬,颜色呈灰、红色。纯白银比重为10.5,熔点961.78℃,导电性能佳,溶于硝酸、浓硫酸中。银的物理和化学性质与周期表第11族中的两个同族元素铜、金相似。其47个电子排列在配置[Kr]4d105s1中,类似于铜([Ar]3d104s 1)和金([Xe]4f145d106s1);第11族是d区块中为数不多,但具有完全一致电子组态的族。
这种独特的电子结构在填满的d副壳层上具有最高占据s副壳银是一种极其柔软、富强韧性和延展性的过渡金属,虽然它比金的稍差。银以面心立方晶格结晶,体积配位数为12,其中只有单个5s电子轨域,类似于铜和金。与具有未填满d壳层的金属不同,银中的金属键缺乏共价特征并且相对较弱。该观察结果解释了单晶银的低硬度和高延展性。
5s层的单个电子,是造成金属银的许多奇异性质的原因。
银具有明亮的白色金属光泽,可以进行高度抛光,其特点是金属本身的名称成为颜色名。与铜和金不同,从填满的d轨域带激发电子到银的s和p导带所需的能量足够大(约385 kJ / mol),它不再对应于可见区域的吸收,而是在紫外线区;因此银是白色的金属。在长于450 nm的所有波长下,受保护的银具有比铝更大的光学反射率。在波长短于450 nm时,银的反射率低于铝的反射率,并在310 nm附近下降到零。
第11族中的元素普遍的具有极高的导电性和导热性,因为它们的单个电子是自由且不与填满的d副壳层相互作用,因为这种相互作用(在先前的过渡金属中发生)降低了电子迁移。[11]银的导电性是所有金属中最大的,甚至比铜还要大,但由于成本较高,因此不能广泛用于该性能。射频工程是一个例外,特别是在VHF和更高的频率,其中镀银改善了导电性,因为这些电流倾向在导体表面而不是通过内部流动。在美国的第二次世界大战期间,13540吨银用于电磁铁富集铀,主要是因为铜的战时短缺。纯银具有最高的任何金属导热系数,尽管碳(金刚石同素异形体)和超流体氦-4的导电率更高。银较任何金属具有最低的接触电阻。
银容易与铜、金以及锌形成合金。具有低锌浓度的锌-银合金可以被认为是银中锌的面心立方固体溶液,因为银的结构不变,而随着添加更多的锌,电子浓度升高。增加电子浓度进一步形成体心立方(电子浓度1.5),复杂立方(1.615)和六方密堆积相(1.75)。
物理性质:
银是11族元素,延展性好(仅次于金),有明亮的银白色金属光泽,抛光度高。在受保护的环境中,银对波长450纳米以上的光波反射率比铝高,对波长450纳米以下的光波反射率不如铝,对波长310纳米的光波反射率降为零。[10]
银的导电性在所有金属中最高,比铜还高,但在电气中由于价格高昂,应用并不广。但射频工程(英语:radio-frequency engineering)是个例外,特别是在甚高频以上的频段,镀银能够显著增加元件和导线整体的导电性,因为高频电流会集中在导体的表面而非内部。二战中美国生产浓缩铀的电磁铁用了13,450吨银,这是因为战时缺铜。
纯银在金属中导热性最高,但低于非金属中的碳(金刚石)和超流体氦-4(英语:superfluid helium-4)。
化学性质:
银是古代发现的金属之一。银在自然界中虽然也有单质存在,但绝大部分是以化合态的形式存在。
银具有很高的延展性,因此可以碾压成只有0.00003厘米厚的透明箔,1克重的银粒就可以拉成约两公里长的细丝。
银的导热性和导电性在金属中名列前茅。
银的特征氧化数为 1,其化学性质比铜差,常温下,甚至加热时也不与水和空气中的氧作用,但久置空气中能变黑,失去银白色的光泽,这是因为银和空气中的硫化氢(H2S)化合成黑色硫化银(Ag2S)的缘故。其化学反应方程式为:
4Ag 2H2S O2 = 2Ag2S 2H2O
银不能与稀盐酸或稀硫酸反应放出氢气,但银能溶解在硝酸或热的浓硫酸中:
2Ag 2H2SO4(浓) —Δ→ Ag2SO4 SO2↑ 2H2O
银在常温下与卤素反应很慢,在加热的条件下即可生成卤化物:
2Ag F2 —473 K→ 2AgF暗棕色
2Ag Cl2 —Δ→ 2AgCl白色
2Ag Br2 —Δ→ 2AgBr黄色
2Ag I2 —Δ→ 2AgI橙色
银对硫有很强的亲合势,加热时可以与硫直接化合成Ag2S:
2Ag S =Δ= Ag2S
类似地,银和硒、碲的反应为:
2 Ag Se → Ag2Se
2 Ag Te → Ag2Te
同位素:
自然界存在的银有两种稳定同位素:107Ag和109Ag,其中前者的丰度略高(51.839%)。银的两种同位素的丰度几乎相同,这在元素周期表中十分罕见(溴是另一个例子)。银的原子量是107.8682 (2) 克/摩尔。
已确定银的二十八个放射性同位素的特性,其中最稳定的依次是105Ag(半衰期41.29天),111Ag(半衰期7.45天),112Ag(半衰期3.13小时)。银有很多亚稳态核素,其中最稳定的依次是108mAg(半衰期418年),110mAg(半衰期为249.79天),106mAg(半衰期8.28天)。其余的放射性同位素的半衰期皆短于一小时,大部分短于三分钟。
银的同位素原子量从92.950(94Ag)到129.950(130Ag)不等。[19][20]丰度最高的稳定同位素(107Ag)之前的同位素的衰变类型主要是电子捕获,生成钯(46号元素)的同位素,而107Ag之后的同位素的衰变类型则主要是β衰变,生成镉(48号元素)的同位素。
107Pd β衰变成107Ag的半衰期为650万年。铁陨石是仅有的“钯-银比”高到可以测量107Ag富度变化的物体。由放射性产生的107Ag首次发现于1978年美国圣塔克拉拉的陨石。
发现者提出,一些小型铁核的行星与其异体,可能是在一千多万年前的核合成事件中产生的。从这熔化过的星球本体中,观察到的107Pd–107Ag比值,反映出早期太阳系的吸积中应存在着不稳定的核种。
银是一种相当不活泼的金属。 因为它填满的4d外壳不能很好地屏蔽从核到最外面的5s电子的静电引力,因此银靠近电位序的底部(E0(Ag /Ag)= 0.799 V)。
在第11族中,银具有最低的第一游离能(显示5s轨道的不稳定性),但具有比铜和金更高的第二和第三电离能(显示4d轨域的稳定性),因此化学银的主要是 1氧化态,反映了随着d轨域填满和稳定,沿过渡系列的氧化态范围越来越有限。
与铜相比,Cu2 与Cu 相比具有更大的水合能 ,这是前者在水溶液和固体中更稳定的原因,尽管后者缺乏稳定的填充d副壳层,银这种效应被其较大的第二游离能量所掩盖。 因此,Ag 是水溶液和固体中的稳定物质,Ag2 在氧化水时稳定性较差。
由于银的尺寸小以及较高的第一游离能(730.8 kJ/mol),大多数银化合物具有显著的共价性。此外,银的鲍林电负性为1.93,高于铅(1.87),其电子亲和力为125.6 kJ/mol远远高于氢(72.8 kJ/mol),并且比氧的 电子亲和力低一些。(141.0 kJ/mol)。
由于其完整的d副壳层,其主要 1氧化态的银表现出相对较少的过渡金属的性质,从4到10族,形成相当不稳定的有机金属化合物,形成线性复合物,显示非常低的配位数,如2,形成两性氧化物以及秦特相,如后过渡金属。与前述过渡金属不同,即使在不存在π-受体配基的情况下,银的 1氧化态也是稳定的。
即使在炙热下,银也不会和空气发生反应,因此和金被炼金术士视为贵金属。 其反应性介于铜(在空气中加热到红热时形成氧化铜(I))和金之间。 与铜一样,银与硫及银的化合物发生反应,在它们存在的情况下,银在空气中失去光泽而形成黑色硫化银(铜形成绿色硫酸盐 ,而金则不反应)。
与铜不同,银金属不会与卤元素反应,除了与氟气形成二氟化物。虽然银不受非氧化性酸的侵蚀,但金属很容易溶于热的浓硫酸,以及稀硝酸或浓硝酸。在空气存在下,特别是在过氧化氢存在下,银容易溶解在氰化物的水溶液中。
历史上银器的三种主要变质方式是失去光泽、长期浸入盐水中而形成氯化银 ,以及与硝酸根离子或氧气反应。 一般情况下,氯化银为淡黄色,暴露在光线下则变成紫色,它从工件或硬币的表面稍微突出。 古银中铜的沉淀可用于制造人工制品,因为铜常是银合金的组成部分。[
银金属受强氧化剂如高锰酸钾(KMnO4)和重铬酸钾(K2Cr2O7)的腐蚀,并且在溴化钾(KBr)存在下。 这些化合物用于照相漂白银图像,将其转换为溴化银,可以用硫代硫酸盐固定或重新开发以增强原始图像。银形成氰化物配位化合物(氰化银),其在过量氰化物离子存在下可溶于水。氰化银溶液用于银的电镀。
银的常见氧化态 (按共性顺序): 1(最稳定的状态;例如,硝酸银,AgNO3); 2(高度氧化;例如,二氟化银,AgF2);甚至是很少见的 3(极端氧化;例如,四氟合银(III)酸钾,KAgF4)。
1状态是迄今最常见的状态,其次是易于还原的 2状态。 3状态需要非常强的氧化剂,例如氟或过二硫酸盐 ,而且有一些银(III)化合物与大气水分和反应并腐蚀玻璃。实际上,氟化银(III)通常经过银或一氟化银与最强的已知氧化剂二氟化氪反应而获得。
特点:
性质稳定,活跃性低氧气相对其他气体能更容易溶解于银。导热,导电率 在常温常压下是所有金属(不包含合金)中最高不易受化学药品腐蚀(但仍然能被硫、硒、硫化物、硝酸、氢碘酸[来源请求]、氯气等腐蚀)质软富有延展性反射率高(银对波长450纳米以上的光波反射率比铝高,对波长450纳米以下的光波反射率不如铝,对波长310纳米的光波反射率降为零。)
应用:
银600-800美元每千克(工业应用必考虑成本,2013年春,相比较铜的价格在8~12美元每千克)。制造高价值的物件如银元货币、首饰,并用于制造勋章、奖座、杯、牌和种种装饰。与汞、锡等其他金属在室温混合成的混合物,被广泛用于牙医上。制造控制棒来控制核连锁反应。用作催化剂,是一种对工业非常重要的催化剂,化学实验室中也会使用。用作电线等导电体,常见于音响设备及键盘。加入镍、铜以增加硬度。在电子工业上是重要的导电材料。制造合金、硝酸银和其它银的化合物等。用作制造镜子反光面。
饰品、精品、工艺品皆有使用。较好的材质为925银,即92.5%银加入7.5%的铜,为 Tiffany & Co.所开创的标准。银能对硫等元素反应,也对某些微生物有*菌功效却对人体无害,加上有美观价值,因此常被做为高级餐具或食物容器。古代也曾有利用这种特性而出现“银针探毒”的验毒技术,但今日已证实银仅对部分元素、化合物及微生物有反应,部分食物如鸡蛋等因含硫即使无毒亦会有反应,验毒功效并非百分之百。
经济用途:
已知最早的硬币是在公元前600年左右在小亚细亚的利底亚(Lydia)王国铸造的;利底亚的硬币是琥珀金(Electrum)制成的,这是一种天然存在的金和银的合金,可在利底亚境内使用。从那时一直到20世纪,白银皆为货币之基准且散布世界各地,其中以白银的固定重量作为标准经济单位。
几个世纪以来著名的银币包括古希腊的德拉克马、古罗马的第纳里乌斯、伊斯兰的迪拉姆、来自古印度喀尔巴那自莫卧儿帝国时代起的卢比(由铜和金币组成)以及西班牙的比赛塔等。用于制造钱币的银量相对用于其他目的的银量随时间波动很大, 例如:在战时,人们往往将更多的银用于制造钱币来为战争提供资金。如今,银的ISO代码为ISO 4217 XAG,是四种贵金属中的一种(其他为钯、铂和金)。
银币由铸棒或铸锭制成,压制成正确的厚度,进行热处理,然后切割取出粗坯。 再将这些粗坯在压模机中研磨和铸造; 现代压铸机每小时可生产8000银币。价值编辑2018年7月,白银的价值约为每公斤495美元,约合每盎司15.5美元。但截至2020年8月6日台北时间17:20,伦敦LBMA金银市场的白银现货价格为每盎司27.7美元。白银价格通常以金衡盎司为单位计算。1金衡盎司等于31.1034克。2015年,中国恢复了公制,目前银和金的价格是以克为单位。伦敦白银价格每天在伦敦时间的中午发布一次。该价格由几家主要的国际银行共同制定,伦敦金银市场成员使用当天价格进行交易。价格通常以美元(USD)、英镑(GBP)和欧元(EUR)显示。
名称由来:
银拉丁原名为argentum,是其化学符号的来源。
因为银的活跃性低,其元素型态易被发现亦易提取,故此在古时的中国和西方分别已被认定为五金和炼金术七金之二,仅于金之后一名。
古代西方的炼金术和占星术也有将金属中的银与七曜中的月连结,又为金和日之后一名。
“银”这个词出现在盎格鲁撒克逊人的各种单字中,例如:seolfor和siolfor。 从德语中可以看到类似的字眼(古高地德语silabar和silbir)。 化学符号Ag来自拉丁语中的银 argentum(古希腊语ἄργυρος),意为“白色”或“ 闪亮的”,这是金属的原始印欧语词汇,无法在德语、巴尔托语和 斯拉夫语中找到此词义。 巴尔托·斯拉夫语对白银的说法与日耳曼语非常类似(例如俄语 серебро及波兰语 srebro,立陶宛语 sidabras)而且它们可能有共同的起源,虽然这是尚未确定的,一些学者猜测以阿卡德语中 sarpu:"精炼 银" 作为这些单字的起源,与sarapu这个词相关(意指改善或冶炼)。
化合物:
1价态化合物编辑银在化合物中主要以 1价的形式存在。银溶于硝酸(HNO3),生成硝酸银(AgNO3)。硝酸银是一种透明晶体,有感光性,且易溶于水。硝酸银是合成许多其他银化合物的原料,也可作为防腐剂,还用于彩色玻璃中的黄色添加剂。银不易与硫酸反应,因此硫酸在珠宝制造中用于清洗银焊及退火后留下的氧化铜火痕(英语:firescale)。
银易与硫以及硫化氢(H2S)反应生成黑色的硫化银(Ag2S),这在失去光泽的银币或其他物品上很常见。当银制电气触点(英语:Electrical contacts)在富含硫化氢的环境下工作时,触点上的硫化银还会生成银晶须。4 Ag O2 2 H2S → 2 Ag2S 2 H2O
向硝酸银溶液中加入氯离子会沉淀出氯化银(AgCl),同样地,加入溴盐或碘盐可以沉淀出用于制造感光乳剂(英语:photographic emulsion)的其他卤化银。氯化银用于制造检测pH值和测量电位的玻璃电极(英语:glass electrode),以及用于玻璃的透明水泥。将碘化银 (AgI)撒入云层以人工降雨。卤化银在水溶液中高度不溶(除了氟化银),因而常用于重量分析。向硝酸银溶液加入碱,沉淀得到氧化银 (Ag2O)。氧化银用作纽扣电池的正极。向硝酸银溶液加入碳酸钠(Na2CO3),沉淀得碳酸银(Ag2CO3)。
2 AgNO3 2 OH− → Ag2O H2O 2 NO3−2 AgNO3 Na2CO3 → Ag2CO3 2 NaNO3雷酸银(AgONC)是一种强烈的、对碰撞敏感的炸药,是银与硝酸在乙醇(C2H5OH)的存在下反应得到的,用于雷管。
其他危险易爆的银化合物包括叠氮化银(AgN3),由硝酸银与叠氮化钠 (NaN3)反应得到,还有乙炔银(Ag2C2),由硝酸银或银氨溶液与乙炔(C2H2)反应得到。卤化银晶体曝光后形成的潜像(英语:Latent image)经还原剂,如氢醌、米吐尔(4-(甲氨基)苯酚硫酸氢盐)或抗坏血酸的碱性溶液显影处理后,曝光的卤化银被还原成金属银。硝酸银的碱性溶液(银氨溶液)可被还原糖,如葡萄糖等还原为金属银,这个反应用于制造银镜,以及玻璃圣诞饰品(英语:Christmas ornament)的内表面。
卤化银可溶于硫代硫酸钠(Na2S2O3)溶液,因此硫代硫酸钠可作为定影剂(英语:photographic fixer),去除显影后感光乳剂上多余的卤化银。[30]在溴化钾(KBr)的存在下,金属银可被强氧化剂如高锰酸钾(KMnO4)或重铬酸钾(K2Cr2O7)侵蚀;这些化合物在摄影中用于漂白可见影像,将其转化为卤化银,既可以被硫代硫酸钠去除,又可以重新显影以加强原始的影像。在过量的氰根离子(CN-)存在下,氰化银(AgCN)可以形成可溶于水的氰配合物(Ag(CN)2-)。银的氰配合物溶液用于电镀银。[30]其它价态化合物编辑银还能形成其它价态的化合物,如氟化亚银(Ag2F)、二氟化银(AgF2)、一氧化银(AgO)等。
在生物中作用:
银的离子以及化合物对某些细菌、病毒、藻类以及真菌显现出毒性,但对人体却几乎是完全无害的。银的这种*菌效应使得它在活体外就能够将生物*死。然而,银制品的测试以及标准化却存在很大难度。希波克拉底曾经有描述银在治疗和防止疾病方面的功用。
腓尼基人曾经用银瓶子来盛放水、酒和醋,以此防止这些液体变坏。20世纪初期,人们也曾把银币放在牛奶,以此来延长牛奶的保鲜期。银的*菌机制长期以来一直为人们所争论探讨,但至此还没有确凿的定论。其中一个很好的例子是微动力效应,成功的解释了银离子对微生物的作用,但却不能解释其对病毒的作用。凝胶以及绷带大量使用银。
银的抗菌性来源于银离子。由于银离子可以和一些微生物用于呼吸的物质(比如一些含有氧、硫、氮元素的分子)形成强烈的结合键,以此使得这些物质不能为微生物所利用,从而使得微生物窒息而亡。在抗生素发明之前,银的相关化合物曾在第一次世界大战时用于防止感染。银作为效用广泛的抗菌剂正在进行新的应用。
其中一方面就是将硝酸银溶于海藻酸盐中,用于防止伤口的感染,尤其是烧伤伤口的感染。2007年,一个公司设计出一种表面镀上银的玻璃杯,这种杯子号称具有良好的抗菌性。除此之外,美国食品和药品管理协会(FDA)最近也审批通过了一种内层镀银的导气管的应用,因为研究表明这种导气管能够有效的降低导气管型肺炎。
银并不会对人的身体产生毒性,但长期接触银金属和无毒银化合物也会引致银质沉着症(Argyria)。因为身体色素产生变化,皮肤表面会显出灰蓝色,虽无毒性,但会影响外观。
总的来说

银
银的主要用途之一是制作硬币和珠宝。在硬币方面,银曾经是世界上许多国家的货币标准之一,而在珠宝方面,银被广泛用于制作各种首饰和饰品。银不仅具有美丽的外观,还因其稳定性而受到青睐。
银还被广泛用于摄影行业。在传统摄影中,银盐是一种光敏材料,被用于制作胶片和相纸。在数字摄影中,银被用作镜头涂层和传感器连接器。
在医学中,银被用于抗菌和消毒。银离子具有*菌作用,因此被用于制造消毒剂和医疗设备。银离子还被用于治疗某些皮肤病和伤口愈合。