下划线内容为高频考点
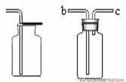
碳酸钠粉末与稀盐酸反应
碳酸钠粉末与稀盐酸反应
(1)实验过程中发生的实验现象:白色固体逐渐较少或消失,溶液中产生大量气泡,天平指针向右偏转。
(2)该反应是否符合质量守恒定律?符合
(3)由此实验,你对测定质量守恒定律的实验在操作上主要注意的问题是:实验中若产生气体,反应应在密闭容器中进行,并且装置没有明显形变,排除浮力等因素对称量的影响。
(4)天平指针向右偏转的原因:碳酸钠和稀盐酸反应生成气体,没有在密闭的装置中进行,气体逸出,没有称量所有生成物的总质量。
(5)反应化学方程式:Na2CO3 2HCl==2NaCl H2O CO2↑
镁条燃烧实验步骤:取一根用砂纸打磨干净的长镁条和一个石棉网,将它们一起放在托盘天平上称量,记录所称质量为W1。在石棉网上方将镁条点燃,充分燃烧后,将燃烧后的产物与石棉网一起放在托盘天平上称量,记录称量后的质量为W2

镁条燃烧
(1)镁条在空气中燃烧的现象:银白色固体燃烧,发出耀眼的白光,放热,冒白烟,生成白色固体。
(2)若反应后果为W1>W2,原因:
坩埚钳上残留一部分氧化镁;
‚随白烟逸散到空气中一部分氧化镁。
(3)如果在燃着的火焰上方罩上罩,使生成物全部收集起来称量,会出现什么实验结果:生成物的质量大于镁条的质量。
(4)在实验中要把镁条用砂纸打磨的原因除去镁条表面的氧化膜
(5)实验中石棉网起到的作用是盛接生成物,防止烫坏实验台。
(6)反应的化学方程式为: