我们已经知道,原子是由居于原子中心的带正电的原子核和核外带负电的电子构成。

我们观察原子的核外电子排布的示意图,复习相关的规律:
通过学习,我们总结出了以下规律:
1.稀有气体元素原子最外层是满的(8个或2个),化学性质比较稳定,很难与其他物质发生反应;
2.非金属元素的原子最外层电子数一般都大于4,容易得到电子;
3.金属元素原子的最外层电子数一般都小于4,容易失去电子。
4.在化学反应中它们都趋于达到稳定的结构,所以最外层电子数与化学性质有关。

小资料:1916年,德国化学家柯塞尔( W. Kossel)根据稀有气体原子的电子层结构具有高度稳定性的事实,提出了“离子键”的概念。认为由原子得失电子后。生成的正、负离子之间靠静电作用而形成的化学键。即离子键的本质是正、负离子之间的静电引力。

那么原子之间是通过什么方式形成离子、进而形成物质的呢?哪些物质是由离子构成的呢?
1-离子形成的过程
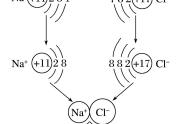
我们以氯化钠和氯化镁的形成为例。
A.氯化钠:
首先我们观察钠原子和氯原子的核外电子排布: