“氢氦锂铍硼,碳氮氧氟氖……”在初识化学元素周期表时,你是否有过这样的疑问:元素周期表应该横着看还是竖着看呢?横着看和竖着看有什么区别呢?

首先从化学元素周期表的发明开始说起,这离不开化学家们的辛苦研究。1803年,英国化学家道尔顿在他的论文中提出了原子学说,首次提出原子量的概念。他认为,不同的原子,不仅大小、形状各异,并且具有不同的质量——原子量。早在1789年出版的《化学大纲》中,法国化学家拉瓦锡就发表了历史上第一张《元素表》。在这张表中,当时已知的33种元素被分为了4类。此后,有多位化学家对元素的性质和分类开展研究。1865年,英国化学家纽兰兹在研究中发现,当元素按原子量递增的顺序排列起来时,每隔8个元素,元素的物理性质和化学性质就会重复出现。他称这一规律为“八音律”。至1869年门捷列夫在彼得堡俄罗斯物理化学学会会议上发表论文,提出他编了一份元素表,表内依照原子量从小到大的顺序排列,元素周期表正式出现。
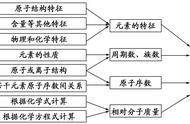
元素周期表中每一种元素都有一个编号,这个编号称为原子序数。原子的核外电子排布和性质有明显的规律性,是按原子序数递增排列,将电子层数相同的元素放在同行,将最外层电子数相同的元素放在同一列。在元素周期表中,横行称周期,用阿拉伯数字表示,有第1、2、3、4、5、6、7周期,其中1、2、3称为短周期,4、5、6称为长周期,第7周期称不完全周期。而纵行称为族,16个族分为7个主族(IA~V II A),7个副族(IB~V II B),1个V III B族,1个零族。(II、III为罗马数字)
同一周期从左到右,元素核外电子层数相同,最外层电子逐渐增多,失去电子能力减弱,获得电子的能力在增强,金属性在减弱,非金属性随之增强。同一主族的元素,其最外层电子数相同,从上到下,元素的核外电子层数依次增加,原子序数递增,金属性在增强,非金属性减弱。
在元素周期表中,元素的位置能反映出元素的核外电子排布,可以对元素性质进行有效推断。所以,无论是横着看还是竖着看,都能够根据其规律得出相应元素性质。
值得一提的是,随着我们对元素规律认知的日益深刻,科学家发现元素周期表存在不少“怪异”之处,有人提出要对现在的元素周期表进行重新设计,并且也已经有了数百个版本的元素周期表。
随着化学的不断发展,新的化学元素会继续填充元素周期表,未来的元素周期表会变成什么样子呢?让我们拭目以待。
(新华网)