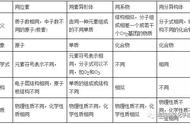
学习目标
1. 同系物的概念
2. 同系物的判断方法
3. 同分异构体的概念
4. 同分异构体的书写和数目的判断
核心知识点一:
一、
同系物
【想一想】
比较下列几种有机物的组成和结构,你能得出哪些结论?

【结论】上述有机物均由碳、氢两种元素组成;除甲烷外均存在碳碳单键,每个碳原子剩余的价键均与氢原子结合;此类有机物,每增加1个碳原子,氢原子数便增加2,故它们在组成上相差一个或若干个CH2原子团。
1. 概念:结构相似,在分子组成上相差一个或若干个CH2原子团的化合物互称为同系物。
2. 结构特点:①符合同一通式(烷烃符合通式:CnH2n 2);
②结构相似;
③组成上相差一个或若干个“CH2”原子团。
3. 性质:因结构相似,故同系物的化学性质相似,物理性质随着碳原子数递增而呈规律性变化,即物理性质不同。(密度、熔、沸点随着碳原子数递增而增大,由于随着碳原子数递增,相对分子质量增大。)
4. 同系物的判断方法
(1)判断标准——“同类不同碳”
同类:互为同系物的有机物均属于同一类物质,即分子结构相似。
不同碳:互为同系物的有机物碳原子数不同,即分子组成上相差一个或若干个“CH2”原子团。
(2)正确理解
①结构相似
a. 结构相似,主要指化学键类型相似,分子中各原子的结合方式相似。
b. 结构相似,则必须符合同一通式,反之不一定成立,如CH2=CH2(乙烯)和
(环丙烷),再比如CH2=CHCH2CH3(丁烯)和
(环丁烷)二者均符合通式CnH2n(n≥2,n为正整数),但结构不相似,不互为同系物。
②组成上相差n个“CH2”原子团(n为正整数)
a. 同系物所含元素种类一定相同
b. 同系物一定具有不同的碳原子数和分子式,即分子式一定不同
c. 同系物一定具有不同的相对分子质量(相差14n,n为正整数)即相对分子质量一定不同。
核心知识点二:
二、同分异构体
1. 概念

二者的分子式相同,都是C4H10,但因碳原子间的连接方式不同导致结构不同(正丁烷是直链结构,异丁烷有支链),故不是同一种物质,它们的物理性质存在一定差异,比如正丁烷的沸点大于异丁烷。

(1)同分异构体要求分子式相同,但结构不同,二者缺一不可;分子式相同,则相对分子质量相等,但相对分子质量相等的物质,分子式不一定相同,如CO和C2H4。
(2)结构不同意味着同分异构体不一定是同类物质,如CH3CH2CH=CH2和
。
(3)同分异构体的结构一定不同,因此它们的物理性质存在差异;如果同分异构体的结构相似,属于同类物质,则它们的化学性质相似;如果同分异构体是不同类别的物质,则它们的化学性质不同。
(4)烷烃中,甲烷、乙烷、丙烷不存在同分异构体,其他烷烃均存在同分异构体,且同分异构体的数目随碳原子数的增加而增多,如丁烷有2种同分异构体、己烷有5种同分异构体。同分异构现象是有机物种类繁多的原因之一。
三、同分异构体的书写与数目判断
1. 烷烃同分异构体的书写方法——“减碳移位”法
“减碳移位法”可概括为“两注意,四顺序”:
两注意:选择最长的碳链为主链,找出中心对称线。
四顺序:主链由长到短,支链由整到散,位置由心到边,排布由对到邻、间。
以书写C6H14的同分异构体为例:
(1)将分子中的全部碳原子连成直链作为主链: