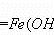本系列文章适合准高一新生进行自学,以及高二高三基础薄弱的同学进行复习
一、概念- 分散剂:分散其他物质的物质,其作用类似于溶剂,例如水溶液中的分散剂为水。
- 分散质:被分散的物质,类似于溶质,例如NaCl溶液中的分散质为NaCl。
- 分散系:分散质分散在水中后形成的体系,例如水溶液。
- 胶体:当分散质的微粒大小在1-100 nm时,该分散系称为胶体。
- 胶粒:胶体的组成微粒,一般带正电或负电。
- 丁达尔效应:当光束照射通过胶体时会形成光亮的通路,该现象称为丁达尔效应。
- 介稳性:胶体的稳定性介于溶液和浊液之间,这种稳定性称为介稳性。
- 聚沉:当外界条件改变时,胶粒之间发生碰撞,聚集在一起发生沉淀的过程。
- 半透膜:一种孔径在纳米级别的膜。
- 透过性:微粒是否透过滤纸或半透膜的性质,由微粒的大小决定。
- 电泳:带电胶粒在电场作用下定向移动的过程。
1、逻辑
- 类似溶质溶解于溶剂形成溶液体系,分散质分散于分散剂中的体系称为分散系;
- 胶体是一种重要的分散系,因其结构的特点而具有多种性质;
- 氢氧化铁胶体是一种常见胶体,由于胶体的一些性质,因此在实验室制备时需要注意细节。
2、应达到的要求:
- 识记常见的胶体
- 区分胶体的本质特征(粒子大小)及其特殊性质(丁达尔效应)
- 理解胶体的若干性质及其在生活中的应用
- 识记Fe(OH)3胶体的制备步骤,书写其方程式

- 胶体区别于溶液的本质特征:粒子大小。(并非丁达尔效应)
- 胶粒表面带电,但是胶体不带电。
- 每个胶粒由多个分子/离子组成,因此胶粒数目远小于原溶液中的分子/离子数。
2.1 丁达尔效应

激光照射溶液与胶体的对比图
- 光照过胶体时形成光亮的通路,而溶液没有,该性质可用于区分溶液和胶体。
2.2 透过性

三种分散系的微粒在滤纸、半透膜中的透过性
- 胶粒的大小为1-100nm,滤纸孔径为μm级,半透膜为nm级,因此胶粒可通过滤纸,不可通过半透膜。
- 溶液中微粒大小<1nm,滤纸和半透膜均可以通过。
- 鉴于溶液和胶体透过性的差异,可利用渗析实现胶体的提纯,如下图所示