"和氢离子"

"结合成水分子。
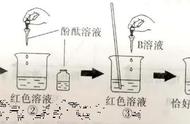
3.C [解析] 结合pH随时间的变化图像,反应开始前pH<7,溶液显酸性,应该是向稀盐酸溶液中滴加氢氧化钠溶液。
4.C [解析] a点时,溶液中有一种溶质H2SO4;稀硫酸与Ba(OH)2溶液反应生成硫酸钡沉淀和水,溶质质量减小,b点时溶液中有硫酸,滴加紫色石蕊溶液,溶液变红;c点时完全反应,溶液pH=7;完全反应后继续加Ba(OH)2溶液到d点,d点溶液中有较多的Ba2+、OH-,无SO42-、H+。
5.D
6.[猜想与假设] 中性(或酸性) 酸性(或中性)
[实验验证] 变红 OH-(或氢氧根离子)
中性(或酸性)
[继续验证] 酸性
Fe2O3+6HCl===2FeCl3+3H2O
无明显现象 中性
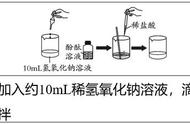
[解析] [实验验证] 因为结论是溶液呈碱性,则滴入的酚酞溶液应变成红色;无色酚酞不变色,只能说明溶液不是碱性溶液,对于是酸性还是中性溶液无法判断。[继续验证] 从图知:是向有酚酞的乙溶液中加入氧化铁,观察到粉末部分或全部消失,溶液变为黄色,说明溶液中有盐酸;如果观察到无明显现象,说明氧化铁没反应,且溶液不呈碱性,则证明溶液呈中性。
7.(1)减小 (2)B
(3)解:设20 g稀盐酸中溶质的质量为x。
NaOH + HCl===NaCl+H2O
40 36.5
20 g×4% x
eq \f(40,36.5)=eq \f(20 g×4%,x)
x=0.73 g
稀盐酸中溶质的质量分数为eq \f(0.73 g,20 g)×100%=3.65%。
答:稀盐酸中溶质的质量分数为3.65%。
PAGE